微波(Microwave)無論在日常生活或是科學研究中已成為不可或缺的工具,其應用範圍不僅限於加熱食物,還涉及各種化學應用。但微波到底是什麼呢?為什麼微波的應用這麼廣?本篇文章將帶您認識微波及其加熱原理,並進一步讓您更清楚了解為什麼微波可以應用於上述各領域。
什麼是微波?
微波是一種低能量電磁波,頻率範圍為1,000~300,000 MHz,其對應的波長範圍為0.001~0.3公尺(圖1)。
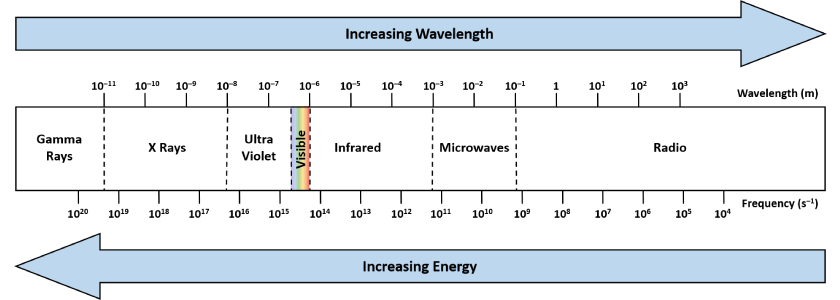
圖1 電磁波譜(Electromagnetic spectrum)
微波與其他電磁波一樣,以互相垂直的電場與磁場在空間中以波的形式傳遞,速度為光速,波的傳遞方向、電場與磁場三者是相互垂直的(圖2)
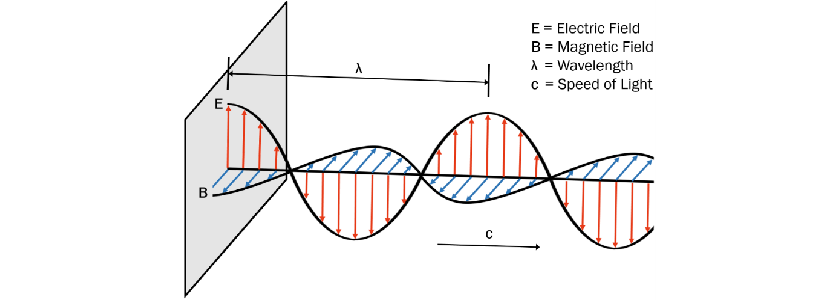
圖2 電場與磁場的示意圖
微波與物質作用時具有三種基本特性,分別為穿透、吸收、反射(圖3)。鐵氟龍、石英…等物質為微波可穿透但不被吸收;極性溶劑如水與丙酮則為微波可穿透且會被吸收;而金屬則為微波無法穿透且不會被吸收的物質。
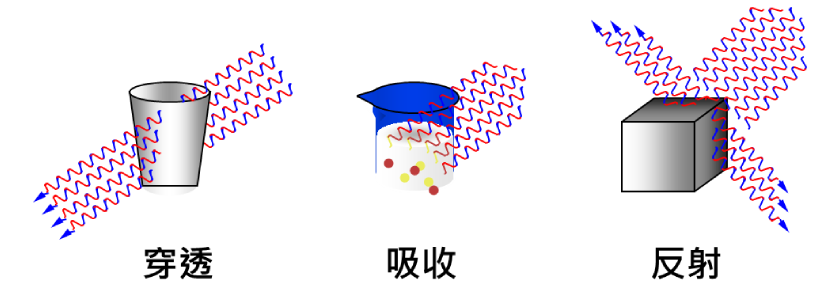
圖3 物質與微波作用的三種特性
微波如何產生熱能?
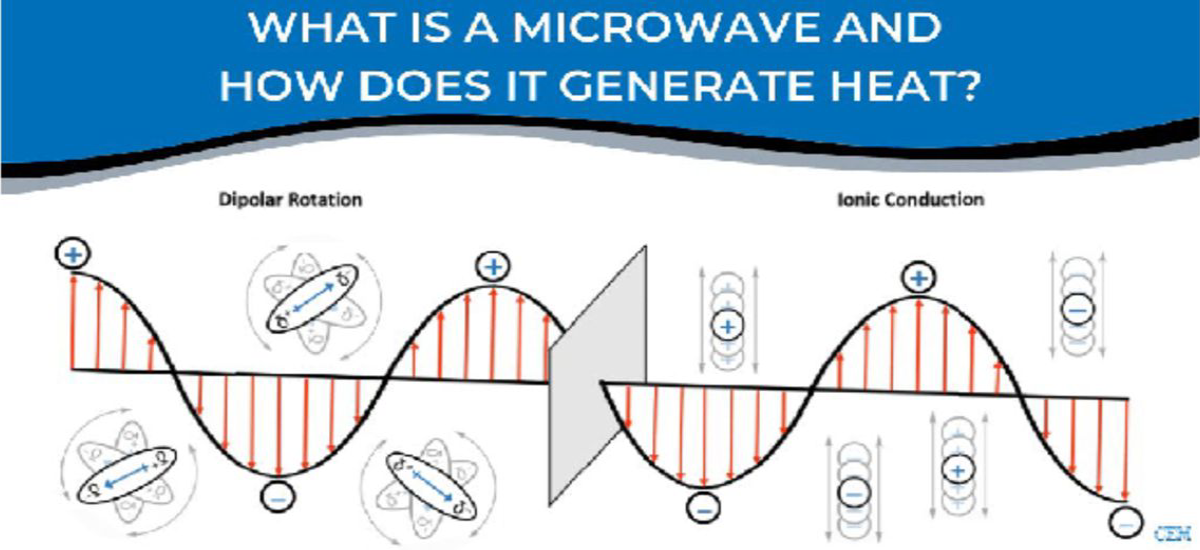
微波加熱的原理為依靠電場的存在,以下列兩種方式與分子相互作用進而產生熱能:
- 偶極轉動(Dipolar Rotation): 分子會不斷地來回轉動,使其偶極子(Dipole)與不斷來回變化與電場的方向對齊,每個旋轉分子之間的摩擦即會產生熱能。
- 離子傳導(Ionic Conduction):一種或多種自由離子在空間中平移,試圖與變化的電場方向對齊。如同偶極轉動方式,這些運動的物質之間摩擦即會產生熱能,反應混合物的溫度越高,能量傳遞的效率就越高。
在這兩種情況下(圖4),極性或離子物種越多,產生熱能的速度則越快。
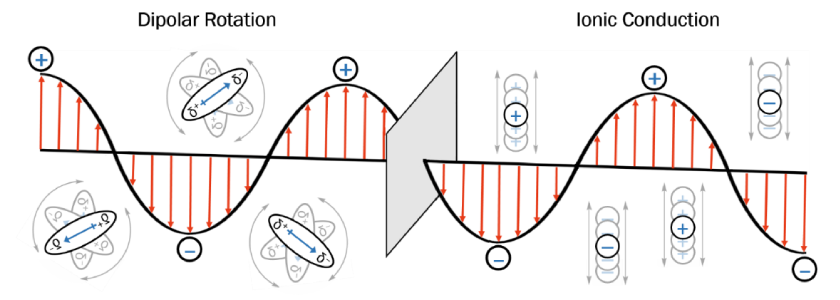
圖4 微波加熱的兩種作用方式:偶極轉動與離子傳導
由圖5可見傳統加熱與微波加熱的示意圖:微波直接與反應物質作用,因此與傳統的加熱技術相比,能量轉移的效率更高。傳統的加熱方法是以熱傳導方式傳遞熱能,其中熱能需先從熱源傳遞到容器,再由容器傳遞到溶液,因此容器表面的溫度往往比溶液高出許多,這會使加熱的效率降低。 微波不以熱傳導方式傳遞熱能,而是透過偶極轉動或離子傳導方式直接加熱溶液中的溶劑與溶質,是一種更有效率與安全的加熱方式。
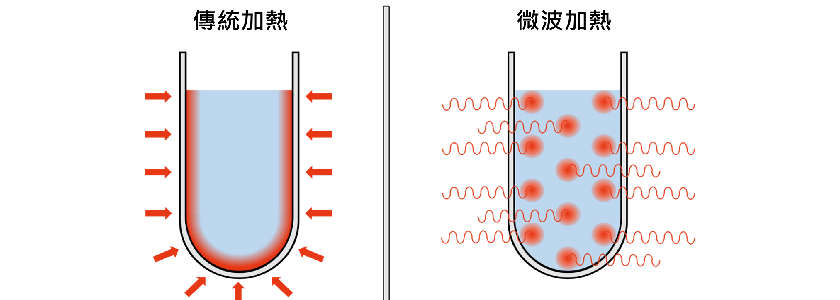
圖5 傳統加熱與微波加熱方式
在化學合成應用中,微波加熱的最大好處為提高反應速率、大幅減少合成時間,以下將介紹微波如何提高反應速率。
微波如何提高反應速率?
要了解微波如何影響反應速率,首先來看化學反應坐標圖(圖6),由圖中可看出化學反應狀態與自由能的關係。反應開始時,反應物(Reactants)處於特定能階( ER)。 為了使反應進行,反應物必須吸收足夠的能量(即熱能)以達到過渡態複合物(Transition State Complex, ETS)的能階。 ETS和 ER之間的能量差稱為活化能( Ea ),一旦克服此能量差,反應物即會迅速形成產物,隨後返回較低的能階EP。
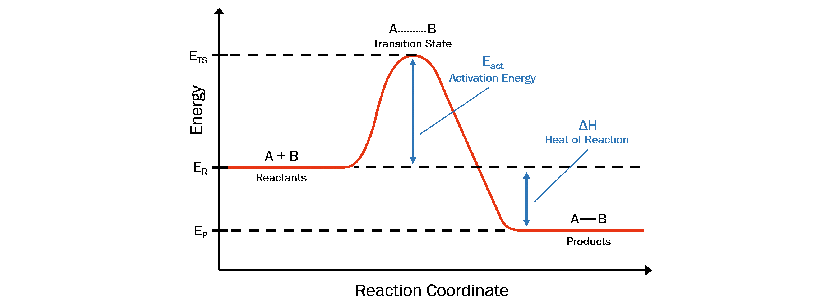
圖6 化學反應坐標圖
接著來看阿瑞尼斯反應速率方程式(Arrhenius reaction rate equation)。
k = Ae-Ea /(RT)(公式1)
Arrhenius方程式為化學反應中速率常數與溫度之間的關係式,由此方程式可看出,微波加熱方式會影響溫度參數(T),溫度的提高會連帶提高反應速率。微波的主要優勢為高效率的產熱方式,當微波吸收能力低的非極性溶劑中存在於微波吸收能力低的極性溶質時,微波加熱方式即可顯著提高反應速度。
以微波反應器進行安全有效率的反應
除了物質與微波能直接相互作用提高加熱速率之外,現今實驗室微波反應器(例如CEM的Discover SP)能在遠高於回流的溫度下進行密閉容器反應,同時也能安全地保持高壓,可安全地於加速反應的條件下進行實驗,提高實驗效率。 由Arrhenius方程式歸納指出,溫度每升高10°C,反應速率約增加一倍。通過這種歸納,可以得出下列公式2中的近似值。
T = T0 + (10°C)x時,t≈(t0)/(2x)(公式2)
其中T為微波加熱溫度,T0 =傳統加熱溫度,x =升溫係數,t =微波加熱時間,t0 =常規加熱時間。由下表1可見傳統加熱反應通常需要花費數小時,而使用微波反應器只需幾分鐘即可完成,溫度每升高10°C,反應速率則增加一倍,所花費的時間則減半。
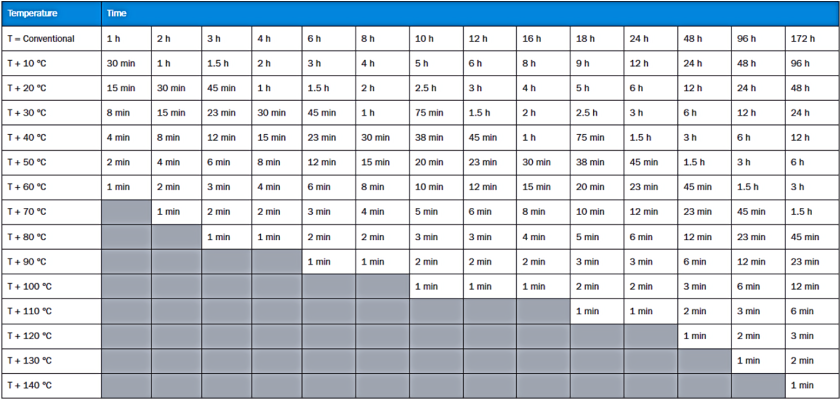
表1 微波反應速率與溫度的關係
微波技術促進科學研究的發展
相較於傳統加熱方式,微波能直接與反應中的物質發生相互作用,提高反應速率,因此微波被應用於許多研究例如:有機合成反應、無機化學的製備、分析化學的應用……針對這些研究也有許多相對應的微波儀器供實驗室使用,微波化學為科學發展提供了良好的動力與應用前景,也大幅增進了研究產能。
欲了解更多的儀器資訊與實驗細節,歡迎來電洽詢 02-2728-2767或 來信與我們聯繫
欲了解更多的儀器資訊與實驗細節,歡迎來電洽詢 02-2728-2767或 來信與我們聯繫
參考文獻
- Galema, S. A. Chem. Soc. Rev. 1997, 26, 233–238.
- Brittany, H. (2002). Microwave Synthesis: Chemistry at the Speed of Light. Matthews: CEM Publishing, pp.11-27.
- Chen P-K.; Rosana, M. R.; Dudley, G. B.; Stiegman, A. E. J. Org. Chem. 2014, 79, 7425–7436.
- Rosana, M. R.; Hunt, J.; Ferrari, A.; Southworth, T. A.; Tau, Y.; Stiegman, A. E.; Dudley, G. B. J. Org. Chem. 2014, 79, 7437–7450.
- Dudley, G. B.; Richert, R.; Stiegman, A. E. Chem. Sci. 2015, 6, 2144–2152.
- Wu, Y.; Gagnier, J.; Dudley, G. B.; Stiegman, A. E. Chem. Comm. 2016, 52, 11281–11283.